|
Tacs又出新概念?一览靶向嵌合体技术发展的新趋势距离耶鲁大学Craig Crews教授团队2008年首次正式提出蛋白水解靶向嵌合分子(PROTAC)概念已过去十余年的时间,相继涌现出各类新型靶向蛋白质降解技术,包括溶酶体靶向嵌合体(LYTAC)技术、自噬靶向嵌合体(AUTAC)技术、自噬小体绑定化合物(ATTEC)技术以及分子伴侣介导的自噬(CMA)嵌合体技术等已在此前的文章中进行了报道。除此以外,还有哪些靶向嵌合体技术值得关注呢?它们相较于PROTAC又有哪些的优势?接下来将逐一为您解析……
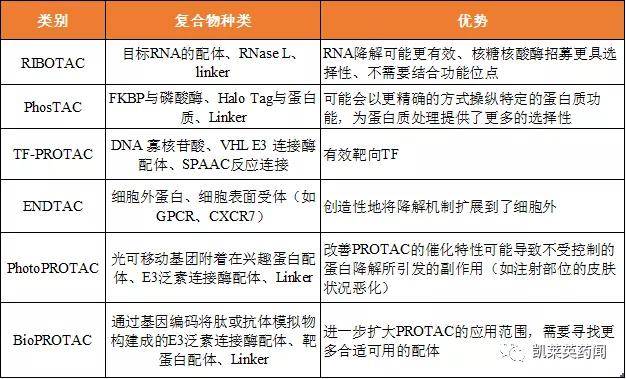
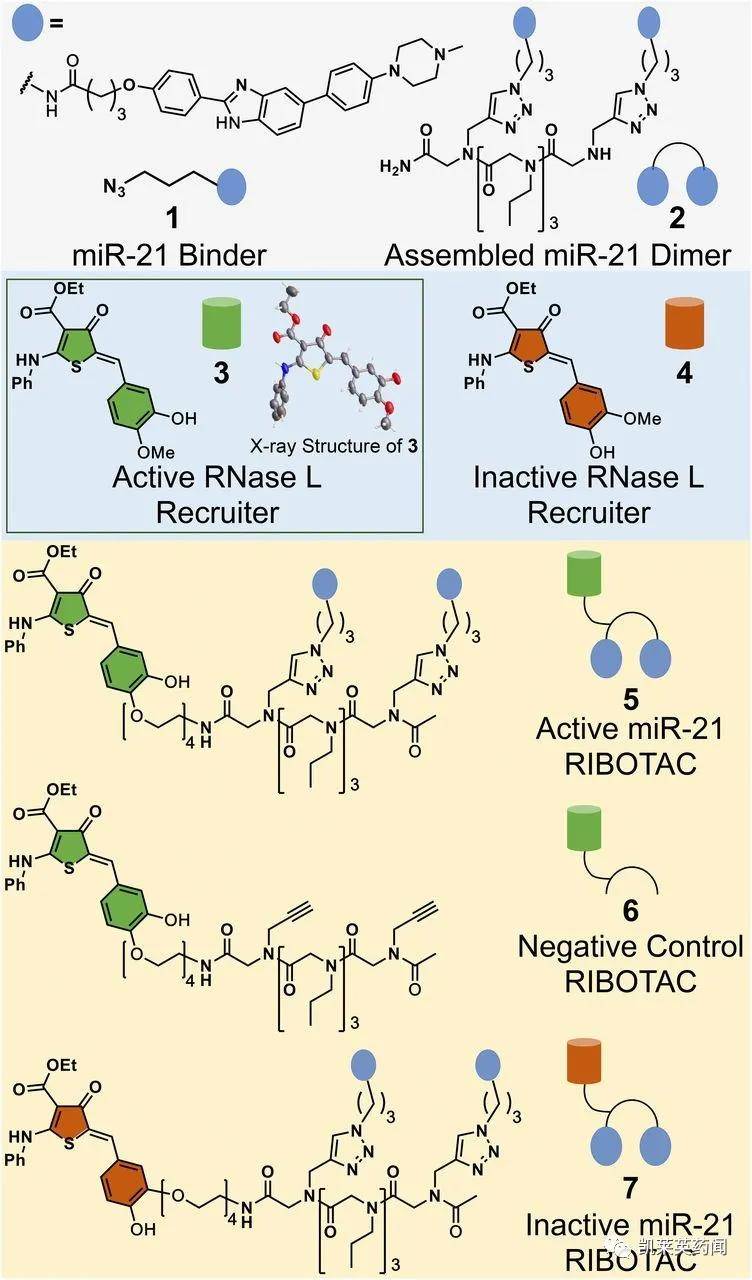
一 RIBOTAC 核糖核酸酶靶向嵌合体(ribonuclease targeting chimeras,RIBOTAC)技术是通过局部招募内源性核糖核酸酶RNase L到特定的转录物上,组装形成二聚体,活化的RNase L选择性降解RNA靶点。该技术的原理与PROTAC类似,连命名也是一脉相承接。通过将所有"玩家"聚集在一个三元复合体(靶RNA:RIBOTAC:RNase L)中,利用细胞内源性的核酸处理机制,局部消除功能异常的RNA,而不是简单地进行结合和抑制。这一技术具有多种优势,如RNA降解可能更有效、核糖核酸酶招募更具选择性、不需要结合功能位点等。
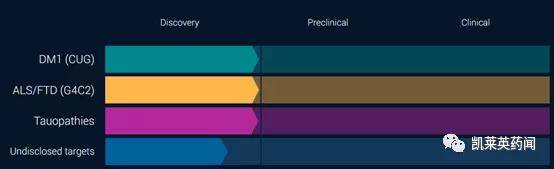
图片来源:PNAS 这项技术最早由美国斯克里普斯研究所的Matthew D. Disney及其团队开发并命名,2018年在线发表在Journal of the American Chemical Society上[1],指出RIBOTAC作用于RNA上,可以选择性地剔除某些基因产物。它的创新之处在于将一种经设计后能够特异性结合RNA的分子,与常见的RNA降解酶结合在一起,这种小分子/酶复合物结合目标RNA后,就可以通过正常的RNA酶的降解作用将RNA降解。为了测试RIBOTAC技术,Disney选择了RNA降解酶RNase L,它是人类抗病毒免疫反应的一个关键部分;RIBOTAC复合物的另一个部分,即药物类似分子,选择了Targaprimir-96,用于与一种已知促进癌细胞增殖(特别是在很难治疗的三阴性乳腺癌中)的microRNA致癌基因(即miRNA-96)结合。研究表明,通过增加FOXO1基因表达破坏miRNA-96会导致癌细胞固有的自毁程重新激活,最终促使这些恶性肿瘤细胞死亡。2021年8月,Scripps Research团队更新了一项最新研究[2],他们将一款酪氨酸激酶抑制剂Dovitinib改造成了靶向RNA的小分子降解剂,对致病RNA的选择性提高了2500倍,并在动物试验中取得了抑制了肿瘤增长的成果。 图片来源:文献[2] 从研究企业上看,Expansion Therapeutics是一家生物技术公司,专注于为严重的RNA介导的疾病(包括神经退行性疾病)开发变革性口服药物。Disney作为Scripps Research的药物化学家,并作为ExpansionTherapeutics的联合创始人,通过汇集了知识产权、专有技术的小分子RNA平台 (SMIRNA™),创造有效的和特定的小分子RNA调节剂。2021年9月,ExpansionTherapeutics宣布完成8000万美元的B轮融资。Cormorant Asset Management领投了此次融资,新投资者Westlake Village BioPartners、Surveyor Capital(一家Citadel公司)和 Logos Capital以及A系列投资者 RA Capital Management、5AM Ventures、Kleiner Perkins、赛诺菲风投和诺华风险基金也参与了此次融资。 Expansion Therapeutics的研发管线(图片来源:官网)
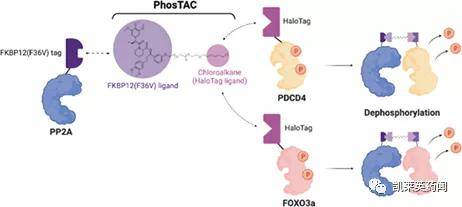
二 PhosTAC 大多数激酶抑制剂靶向激酶的ATP结合位点,它们通常也会和其他激酶的相互作用而表现出脱靶毒性。因此,迫切需要开发一种替代策略来靶向临床应用中失调的激酶。近期,PROTAC概念的提出者Crews,再次提出了靶向蛋白去磷酸化嵌合体 (PhosTAC) 的概念并进行验证性研究[3]。PhosTACs专注于将FKBP与磷酸酶融合,Halo Tag与底物蛋白融合,在加入对应的PhosTAC复合体之后,即可介导底物的去磷酸化。与PROTAC引起的功能丧失不同,靶向蛋白质去磷酸化可能会以更精确的方式操纵特定的蛋白质功能,为蛋白质处理提供了更多的选择性。研究人员证明了PhosTAC可以介导三元复合物形成,并且可以诱导PDCD4和FOXO3a的去磷酸化,且FOXO3a的去磷酸化具有可测定的生物学意义。
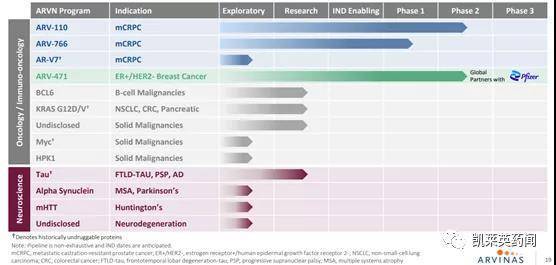
图片来源:文献[3] 从研究企业上看,Crews是Arvinas的股东和顾问,此外也是Halda Therapeutics的创始人。作为靶向蛋白质降解技术的先驱,目前Arvinas已将多个蛋白质降解剂推进临床,近期更新了与辉瑞联合开发的核心药物ARV-471治疗局部晚期或转移性ER阳性/人表皮生长因子受体2(HER2)阴性(ER+/HER2-)乳腺癌患者的I期安全性和有效性数据,并预备在2021年12月圣安东尼奥乳腺癌研讨会(SABCS)上公布试验情况;而Halda Therapeutics作为一家处于研究阶段的药物发现公司,于2019年初和2020年11月分别获得了初始资金和A轮融资,目前尚未对外公布研发管线。 Arvinas的研发管线(图片来源:官网)
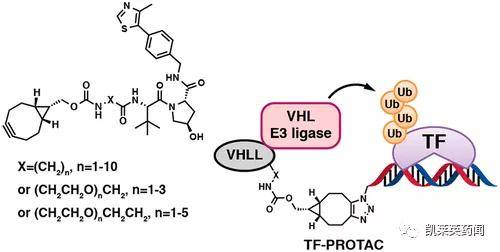
三 TF-PROTAC 转录因子 (TF) 代表了一类主要用于治疗包括癌症在内的人类疾病的治疗靶点。它能与基因5`端上游特定序列专一性结合,从而保证目的基因以特定的强度在特定的时间与空间表达的蛋白质分子。尽管大多数TFs的生物功能和结构已经明晰,但由于它们缺乏通常存在于激酶或其他酶类的活性位点或变构调节的口袋,一些使用小分子抑制剂靶向TF的治疗性干预措施未能实现有效靶向。2021年6月,哈佛大学医学院病理学教授Wenyi Wei团队发表了相关的论文[4],将DNA寡核苷酸与E3连接酶配体连接构建了基于VHL的TF-PROTACs平台,即NF κB-PROTAC (dNF-κB) 和 E2F-PROTAC (dE2F),它们分别有效地降解细胞中的内源性p65和E2F1蛋白,并表现出优越的抗细胞增殖的作用。
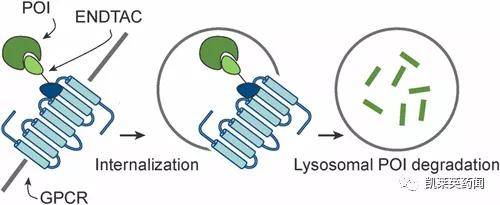
图片来源:文献[4] 从研究企业上看,Wenyi Wei是Rekindle Therapeutics的联合创始人和股东,Rekindle Therapeutics是一家生物技术公司,目前暂未对外公布研发管线。而文章的另一位通讯作者金坚则是睿跃生物(Cullgen)的联合创始人和股东。睿跃生物基于其专有的 uSMITE™ 靶向蛋白质降解技术平台开发小分子疗法,建立了多个靶向蛋白降解剂的疾病治疗管线项目,目前尚未对外公开。2021年2月,Cullgen宣布已完成5000万美元的B轮融资。 四 ENDTAC Crews在2019年5月公布了一种称为“内源性嵌合体”(ENDTAC)的双特异性小分子[5]。ENDTAC的一端可结合细胞外的靶点蛋白,另一端可结合细胞表面受体(如 GPCR、CXCR7),这种分子通过将需要降解的细胞外蛋白与细胞表面的受体连接起来,触发内吞过程,将靶点蛋白“吞入”细胞中,通过溶酶体降解。与使用UPS的PROTAC相比,ENDTAC创造性地将降解机制扩展到了细胞外,不过,该技术虽然有望应用于与胞外蛋白质降解有关的疾病研究,但其应用性和实用性仍然需要进一步优化。
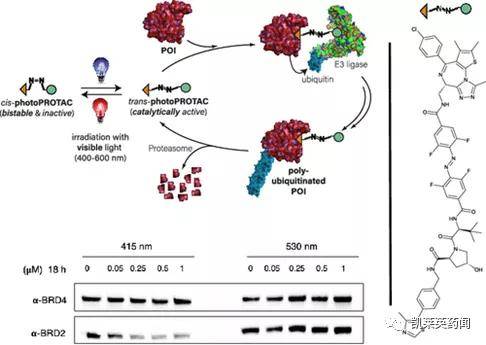
图片来源:文献[5] 五 PhotoPROTAC 基于双功能小分子PROTAC的成功原理,苏黎世大学Patrick Pfaff团队[6]通过在两个弹头配体之间加入邻位F4-偶氮苯连接体来设计光可切换PROTAC (photoPROTAC),用于改善PROTAC的催化特性可能导致不受控制的蛋白降解所引发的副作用(如注射部位的皮肤状况恶化)。PhotoPROTAC是第三代可控的PROTAC,其引起的目标蛋白降解可以由UVA或可见光触发。在photoPROTAC中,一个光可移动基团附着在兴趣蛋白配体或E3泛素连接酶配体或连接器上,比起传统的PROTAC,在降解蛋白时更加精准可控。该项研究得到了苏黎世联邦理工学院的资金支持,Crews依旧为发表文章的通讯作者。
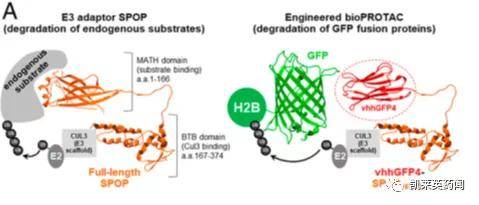
图片来源:文献[6] 六 BioPROTAC 为了进一步扩大PROTAC的应用范围,需要寻找更多合适可用的配体。研究者们[7]应用基因工程技术,通过基因编码将肽或抗体模拟物构建成E3泛素连接酶,用于降解靶蛋白,并将这种技术称之为基因编码靶向蛋白降解(BioPROTAC)。BioPROTAC通过增殖细胞核抗原 (PCNA) 以引起快速和稳健的PCNA降解以及对DNA合成和细胞周期进程的相关影响,在细胞中表达以驱动POI的靶向降解。这种技术可以指导选择最合适的E3连接酶,但由于这种技术依赖于基因编码,因此仅限于开展化学生物学相关研究应用。该项研究成果由基因泰克公司编辑,2020年2月发表于美国科学院院报。
|