|
两种冷冻电镜新技术综述|MicroED和SPA技术对比结构生物学对于生物技术、药物发现等许多领域都大有裨益,是当今生物学界的研究热点。在结构生物学领域,最富传统意义的结构解析方式是X射线晶体学(X-ray crystallography),其研究对象是内部质点具有规则排列性质的晶体。但此方法必须以具有高质量的大尺寸晶体作为前提。然而得到质量较好的晶体对于分子量巨大或者结构柔性的对象来说往往较为困难,尤其是针对膜蛋白这一目前科研人员很感兴趣的对象,其结晶难度更大。为了解决这一问题,基于冷冻电子显微镜的衍生出了两种重要的结构生物学技术手段——单颗粒分析技术(single particle analysis,SPA)和微晶电子衍射技术(Micro electron diffraction,MicroED),本文将对这两种技术的原理和技术特点进行介绍和对比分析。 在过去十几年间,SPA和MicroED冷冻电镜技术有了长足的发展,正在迅速地超越X射线晶体学,成为研究大分子结构的首选方法。2017年,Jacques Dubochet、Joachim Frank和Richard Henderson因冷冻电镜单颗粒法方面的工作而被授予诺贝尔化学奖;
2018年,MicroED被国际权威Science杂志评选为年度全球十大科技进展之一,共同入选的还有应用RNA干扰(RNAi)技术的基因沉默药物、单细胞测序追踪单细胞发育谱系等十项生命科学、物理、化学等领域中的全球顶尖成果。 冷冻电镜SPA介绍 SPA原理和发展历史: 单颗粒分析技术利用的是电子显微镜的成像性质。通过将生物大分子的溶液样品快速投入至冷却到液氮温度的液态乙烷中,得到冰层厚度合适的冷冻样品,然后对冰层中均匀分布的生物大分子颗粒进行拍照。通过算法对拍到的上千张不同角度的二维照片进行分析,最终得到蛋白结构,此方法称之为单颗粒分析技术(single particle analysis)。因此单颗粒分析技术是对冰层中的样品颗粒进行成像,不需要X射线晶体学所需的晶体。其测试过程示意图如下,正式进行样品观察和数据收集之前,样品还需进行负染筛选,从而得到均一性高的样品,负染筛选过程一般在200KV的透射电镜上进行,正式的数据收集需要在300KV的透射电镜上进行。得到二维照片之后还需要经历图像的预处理,目标样品颗粒的提取和筛选以及蛋白的三维重构,最终得到蛋白的3D模型。
目前,单颗粒分析技术的分辨率已经达到了近原子水平(约3Å水平),用该方法解析出的生物大分子三维结构所占的比例越来越大,而且众多过去无法解析的无对称重要生物大分子结构也被解析出来。归纳起来,单颗粒法的发展得益于以下技术的发展:
SPA不足Disadvantages
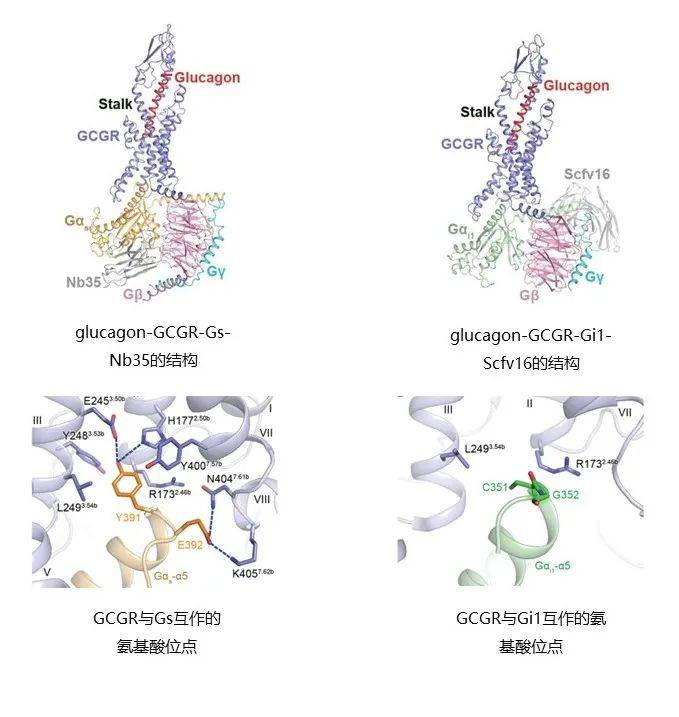
SPA案例 单颗粒分析技术不需要得到晶体且样品使用量非常少,这使得针对难以结晶的蛋白或大分子复合物的研究成为可能。如膜蛋白、抗体-抗原表位鉴定、AAV衣壳等等。 2020年3月发表在Science杂志的研究通过冷冻电子显微镜单颗粒分析技术,确定了与胰高血糖素及不同类别的异源三聚体G蛋白(Gs或Gi1)结合的人源胰高血糖素受体(GCGR)3.7 Å和3.9 Å的结构。该研究的多个结构与药理学数据相结合,为II型糖尿病和肥胖症的治疗提供了重要见解1。
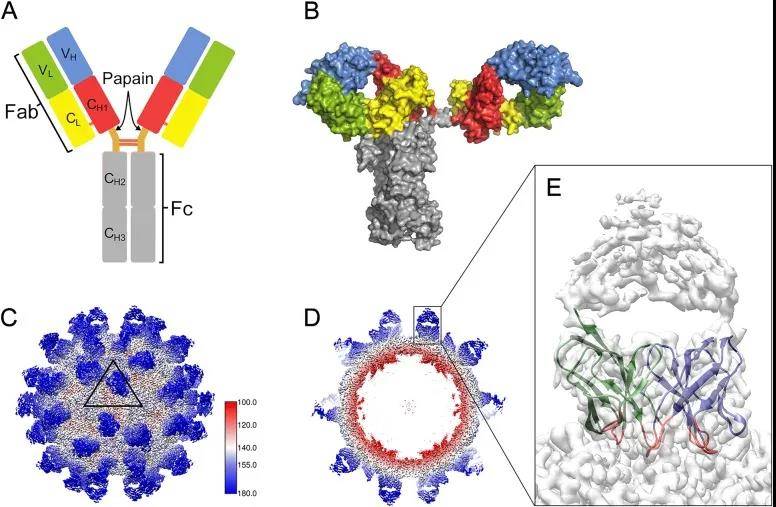
抗原表位即抗原决定簇,是由连续或者不连续氨基酸组成的蛋白质三维结构,其特殊三维结构所包含的线性表位和构象表位以及化学特性决定了抗原决定簇的抗原特性。Li等人通过冷冻电镜SPA解析得到了HPeV3 (EMD-0069)病毒表面抗原决定簇和与抗体结合后复合物的三维结构2,结构示意图如下所示。
MicroED介绍 MicroED原理 根据衍射的原理,只要具有波的性质,就能对晶体产生衍射。电子波同 X 射线一样,照射到类似晶体的样品上时也能够发生衍射现象。所以以电子波为光源的电子显微镜除了成像模式外,还有衍射模式。当中间镜的物平面位于物镜的后焦面时,将在荧光屏上得到经中间镜和投影镜放大了的电子衍射谱,即为透射电子显微镜的衍射模式。通过电子对微小的晶体进行衍射,收集电子衍射数据并进行蛋白质结构解析的方法被称为MicroED。其测试过程示意图如下:
MicroED特点 1. 分辨率高,由于电子的波长比X射线的波长更短,则受物质散射强(原子对电子的散射能比 X 射线强一万倍),所以在理论上能够达到更高的分辨率。 2. 纳米晶体、蛋白质晶体培养难度大大降低。电子衍射在许多方面类似于X射线衍射,同样依赖于有序的晶体,但MicroED所需的晶体样品只要求百纳米3,比传统 X 射线晶体学所需的晶体体积小数十亿倍4。一方面是因为与X射线相比,电子与原子相互作用的散射截面要大得多5,电子与物质的相互作用也强得多(原子对电子的散射比 X 射线强一万倍), 另一方面是因为非弹性散射释放到样品上的能量更少5, 所以微米尺寸的晶体就可以产生足够高的信噪比衍射信号。 3. 样品不能过厚。当晶体大于3 μm时,电子束将无法穿透样品,不会产生衍射信息。考虑到电子的平均自由程,晶体的厚度直接决定了衍射数据的质量6。对于300 kV加速电压得到的电子,其冷冻生物样品的平均自由程约为350 nm,而对于200 kV加速电压得到的电子,其平均自由程约为 300 nm7。过厚的晶体会更频繁的吸收电子,产生更多的多次弹性散射。4. 浸泡成功率高。靶标蛋白-小分子药物配体的共晶结构是药物设计过程中最关键的信息,共晶复合物往往通过浸泡的方法获得。小分子更容易进入纳米级别尺寸的晶体,且更不易产生晶体破裂等情况,大幅提高浸泡成功率。5. MicroED对设备的要求较低,相对低端的透射电镜也能实现高分辨率的电子衍射数据采集,几分钟即可完成一套数据的收集,即使需要多套数据合并,也能在几个小时内完成,实现快速和高通量测试。 MicroED案例分享 在MicroED发展初期,溶菌酶、catalase和 Ca2+-ATPase等模式样品就被解析到原子分辨率。随着MicroED的进一步发展,这项技术不再局限于解析模式样品,来自于瑞典的斯德哥尔摩团队还解析了α-synuclein中心肽段和R2lox酶8等未知蛋白的结构(见下图),并且分辨率都高达~1 Å。
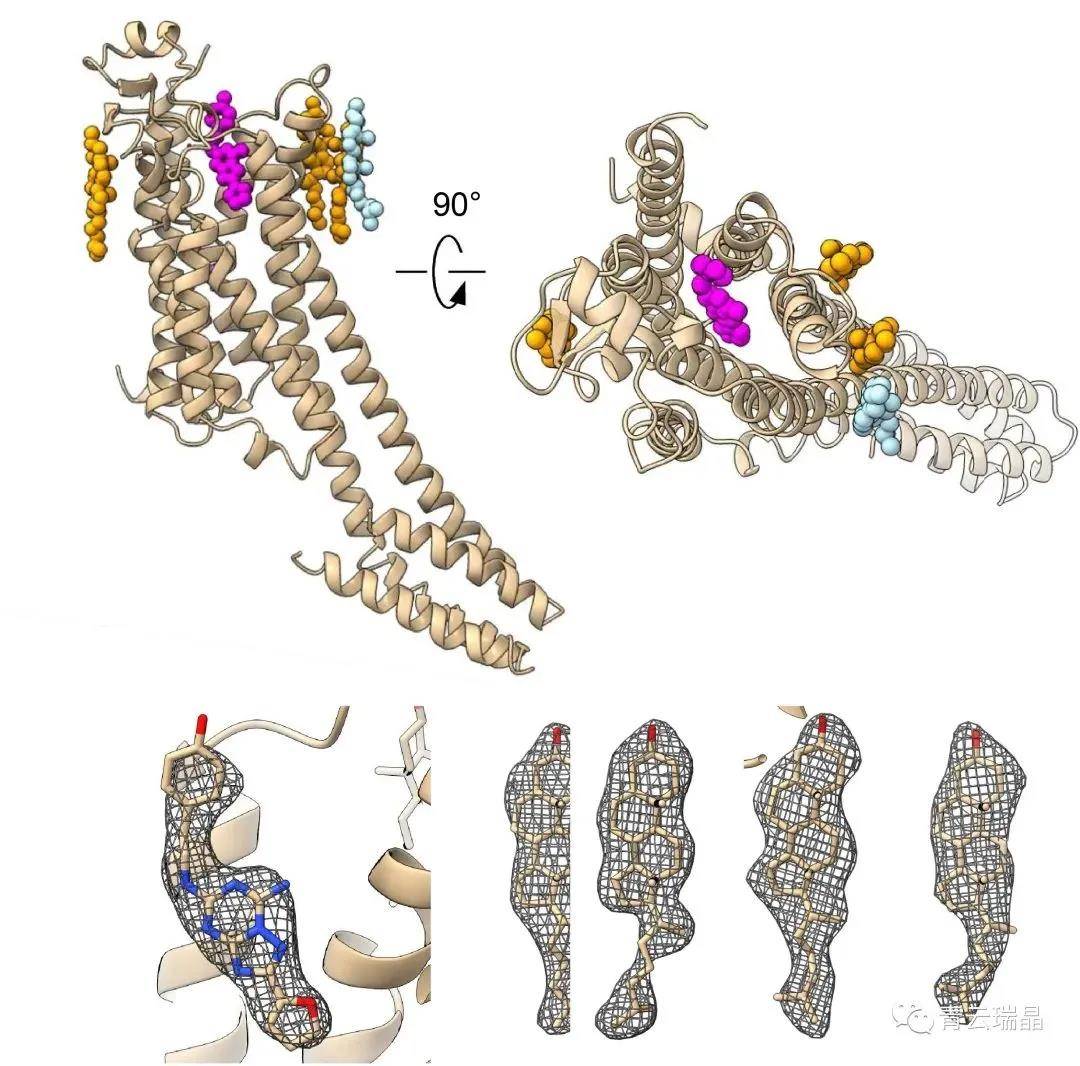
MicroED解析的R2lox结构图 2016年后,MicroED发展迅速,解析的蛋白质结构的数量也随之快速增加,prions和 FUS LC(fused in sarcoma low-complexity domain)等样品的晶体结构都得到了1 Å左右的高分辨率。而后MicroED解析对象的难度逐渐增加,甚至还包括了复合物和离子通道等膜蛋白,下图便是MicroED技术解析的GPCR蛋白A2AR。
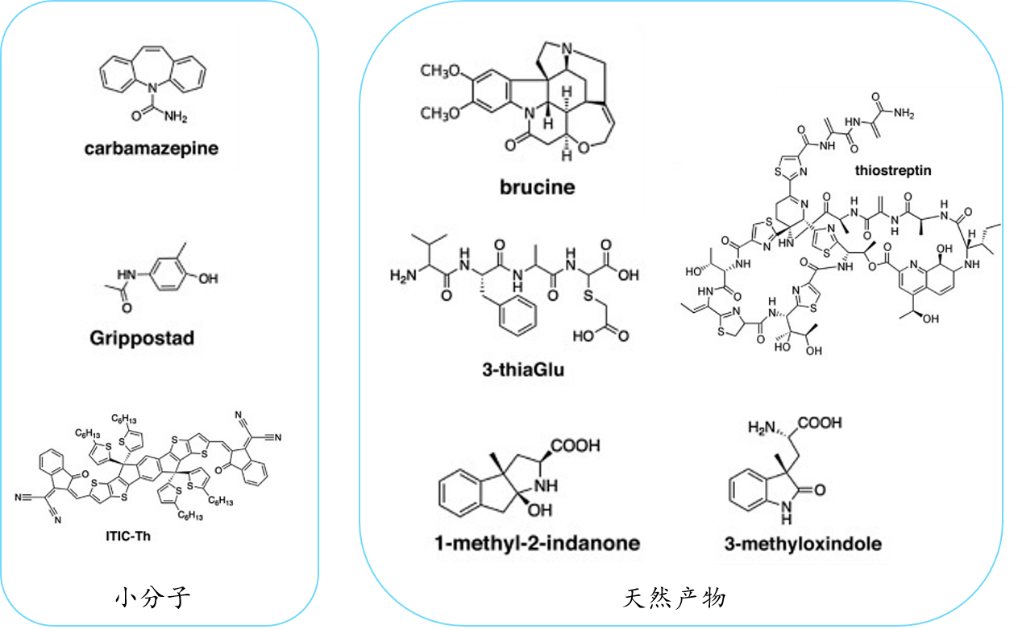
MicroED技术解析的膜蛋白A2AR结构9 除了生物大分子之外,MicroED对化学小分子、天然产物、药物制剂的研究更加合适。因为化学小分子呈现粉末状,尺寸上与其的研究范围非常契合,很多利用MicroED研究化学小分子的成功案例都验证了此技术的高效性和应用性(见下图)。
MicroED得到的化学小分子及天然产物的案例10 |